|
Utilisation d'un calorimètre
en STS maintenance |
Marc Faucompré
Rappel du référentiel du BTS maintenance :
Il est demandé
dans la partie savoir-faire expérimentale en thermodynamique : "Utiliser un
calorimètre pour mesurer une quantité de chaleur". En plus, dans la partie
savoir-faire théoriques, il est demandé "écrire et exploiter des équations
calorimétriques".
Objectifs du TP
Utiliser un calorimètre et exploiter des
équations calorimétriques pour déterminer
- la capacité thermique Ks d'un
système
- la capacité thermique massique c d'un métal
Matériel utilisé
- 1 calorimètre avec résistance chauffante
et agitateur
- 1 thermomètre 0°C - 60°C, gradué au 1/10ème de degré
- 1
alimentation continue
- 1 cylindre d'aluminium de masse environ égale à
60g
- 1 éprouvette graduée
- 1 bain marie thermostaté (pour le chauffage
du cylindre d'aluminium)
- 1 balance électronique
- 1 voltmètre et un
ampèremètre
Ce TP est prévu pour une séance de 2
heures.
I- Présentation du calorimètre
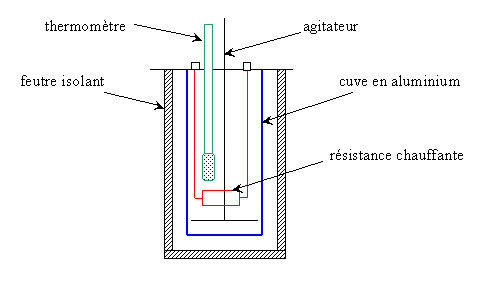
Le calorimètre utilisé est constitué d'une cuve en aluminium placée à
l'intérieur d'un récipient isolé thermiquement par du feutre. L'ensemble
comporte un thermomètre et deux résistances chauffantes identiques, de 20W chacune, montées en série.
Dans cette étude
expérimentale, on tiendra compte de la capacité thermique du calorimètre.

II Energie thermique produite par la résistance chauffante
On souhaite déterminer l'énergie thermique dissipée par une résistance
électrique dont la valeur ohmique dépend quelque peu de la température de
fonctionnement.
Pour cela, on effectue les opérations suivantes :
*
Remplir le calorimètre avec 200mL d'eau prise à température ambiante
*
Placer la résistance chauffante à l'intérieur du calorimètre
* En alimentant
les résistances chauffantes sous une tension continue U= 30V, relever
l'évolution de l'intensité du courant d'alimentation I en fonction du
temps t pendant une durée totale de 8 minutes (on effectuera les mesures
toutes les 30s)
* Déterminer l'expression de l'énergie thermique Wth dissipée
par la résistance en fonction de U, I et t
* Tracer, sur
papier millimétré, la courbe Wth = f(t).
III- Capacité thermique du système (calorimètre + eau)
On souhaite étudier expérimentalement la capacité thermique du système (calorimètre+instruments+ eau). Pour cela, on effectue les opérations suivantes
1- a- Remplir le calorimètre avec 200mL d'eau prise à
température ambiante puis attendre que le système soit à l'équilibre
thermique.
b- En vous aidant de la courbe WTh = f(t),
déterminer le temps de fonctionnement tf des résistances chauffantes pour qu'une
énergie égale à 10kJ. soit fournie au système
c- En alimentant
les résistances chauffantes sous 30V pendant la durée tf, relever
l'évolution de la température q (en degré
Celsius) en fonction du temps t pendant une durée totale de 12 minutes
(on effectuera les mesures toutes les 30s).
Remarque : Pour cette expérience, il faut impérativement agiter l'eau contenue dans le calorimètre afin que la température soit uniforme dans le liquide.
d- Tracer, sur papier millimétré, la courbe d'évolution de la
température q en fonction du temps
t.
e- Commenter l'allure de cette courbe et déterminer
la valeur de la capacité thermique Ks de l'ensemble du
système.
f- Pourquoi la température diminue-t-elle lentement
après l'arrêt du chauffage?
2- Reproduire les manipulations
précédentes pour un volume d'eau initial de 400ml. La nouvelle valeur de la
capacité thermique du système sera notée Ks'.
3-
a- Exprimer la capacité thermique Ks en fonction de la
capacité thermique massique de l'eau ce, la capacité thermique du
calorimètre Kc et la masse d'eau me.
b- A partir
des valeurs de Ks et Ks' trouvées précédemment, calculer les
valeurs de ce et Kc.
IV Détermination expérimentale
de la capacité thermique massique de l'aluminium
Pour déterminer la valeur de la capacité thermique cal de
l'aluminium, on réalise le protocole suivant :
* Remplir le calorimètre avec
200mL d'eau prise à température ambiante qa.
* Introduire dans le calorimètre un
cylindre d'aluminium, chauffé au préalable à qAl = 60°C, puis mesurer la nouvelle
température d'équilibre thermique qf.
Préciser le temps au bout duquel on peut mesurer qf
* En écrivant l'équation calorimétrique
correspondant à cette expérience , déterminer la capacité thermique du cylindre
d'aluminium KAl.
* Mesurer, à l'aide d'une balance électronique, la
masse du cylindre d'aluminium. En déduire la valeur expérimentale de la capacité
thermique massique de l'aluminium. Comparer ce résultat avec la valeur donnée
par une table : cal = 895 J.kg-1.K-1.
Quelles sont les causes d'erreur
?
Marc Faucompré